¿Qué es el jabón?

El jabón se conoce desde hace miles de años. Tanto es así, que los restos más antiguos que se conservan se encontraron en Irak –antigua Babilonia- y datan de 2.800 aC.
La palabra “jabón”, sin embargo, procede del latín “sebum” y significa grasa. Y es que cuenta la leyenda que los romanos sacrificaban animales en el “Monte Sapo” y que, cuando llovía, los restos de grasa animal se mezclaban con las cenizas de los fuegos que habían encendido para hacer los sacrificios. Después la misma lluvia arrastraba esta mezcla desde la montaña al río, dónde generaba una espuma que ayudaba a limpiar las manos, el pelo, la ropa…
¿Cómo funciona el jabón?
¿Pero cómo puede ser que la grasa animal, simplemente mezclada con cenizas, se convierta en un agente capaz de limpiar? La respuesta nos la da la química.
Tal y como hemos visto, la grasa es lo que se conoce como un triglicérido, y tiene, de manera general, la siguiente estructura:
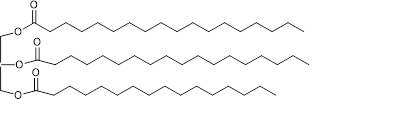
Estructura de una grasa o triglicérido
Por otra parte, hemos dicho que cuando ésta grasa se mezcla con la ceniza se genera el jabón. ¿Qué tiene la ceniza que permite esta transformación de la grasa?
La ceniza contiene varios compuestos entre los cuales están los carbonatos y los hidróxidos de sodio y potasio. A este tipo de compuestos se les llama “alcalinos” y son capaces de romper la estructura del aceite.
Bajo un punto de vista químico, ha tenido lugar la siguiente reacción: la grasa se ha roto y se ha formado una “sal sódica o potásica de un ácido graso” -es decir, el jabón-. A esta reacción se la conoce en química como reacción de saponificación.
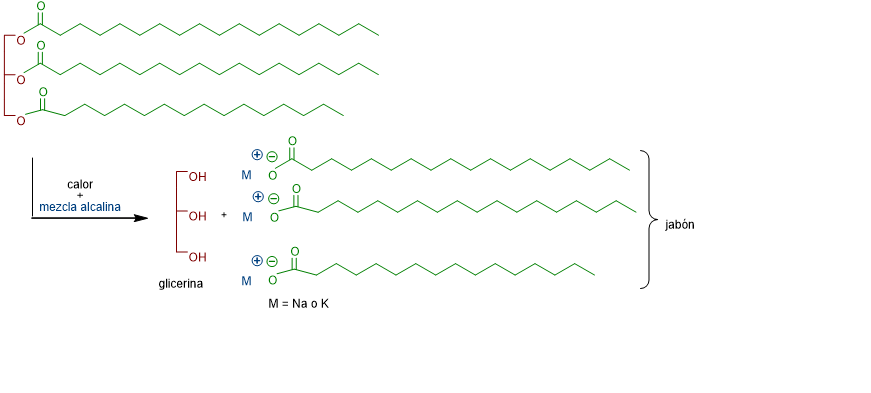
Reacción de saponificación
De esta forma, la grasa inicial se ha transformado en 3 compuestos que contienen 2 partes: una soluble en agua o polar -que es la parte con cargas- y otra soluble en aceite o apolar–que es la parte de las cadenas en zig-zag-. La figura siguiente es la representación de este tipo de moléculas, con una cabeza polar y una cola apolar:
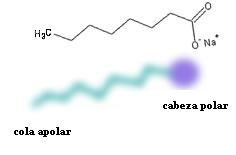
Representación de una molécula polar-apolar
Un subproducto resultante de esta reacción es la glicerina, que tiene un gran poder hidratante y lubricante y varias aplicaciones tanto en la industria cosmética, como en la farmacéutica o la alimentaria.
Volviendo al jabón, un detalle importante es que, la reacción puede tener lugar calentando la masa o a temperatura ambiente. En el primer caso, la reacción de saponificación es más corta, 2 ó 3 días, pero los compuestos más lábiles pueden llegar a degradarse. En cambio, si la reacción se lleva a cabo a temperatura ambiente, habrá que esperar un mes para poder utilizarlo pero así se aseguran todas las propiedades de sus componentes.
Pero ¿por qué el jabón es capaz de arrastrar la grasa?
Sabemos que la grasa no es soluble en agua. Pero cuando aplicamos una mezcla de agua y jabón a una superficie sucia, las moléculas de jabón consiguen “juntar” la grasa y el agua. Por un lado, son capaces de interaccionar con la grasa, y por el otro, con el agua, de manera que consiguen separar la suciedad de la superficie – ya sea pelo, piel, ropa- y dejarla limpia.

Esquema de la extracción de la suciedad por un jabón

Artículo escrito por:
Gisela Saborit Villarroya es Doctora en Quimica Orgánica. Ha trabajado en la empresa biotecnológica Prelude Therapeutics (Delaware, EEUU) y actualmente está en Clarivate Analytics (Barcelona) como analista de síntesis orgánica.
